Při studiu chování plynů ve fyzice je velká pozornost věnována izoprocesům, tedy takovým přechodům mezi stavy systému, při kterých je zachován jeden termodynamický parametr. Mezi stavy však dochází k přechodu plynu, který není izoprocesem, ale hraje důležitou roli v přírodě a technologii. Jedná se o adiabatický proces. V tomto článku se jím budeme zabývat podrobněji a zaměříme se na to, co je adiabatický exponent plynu.
Adiabatický proces
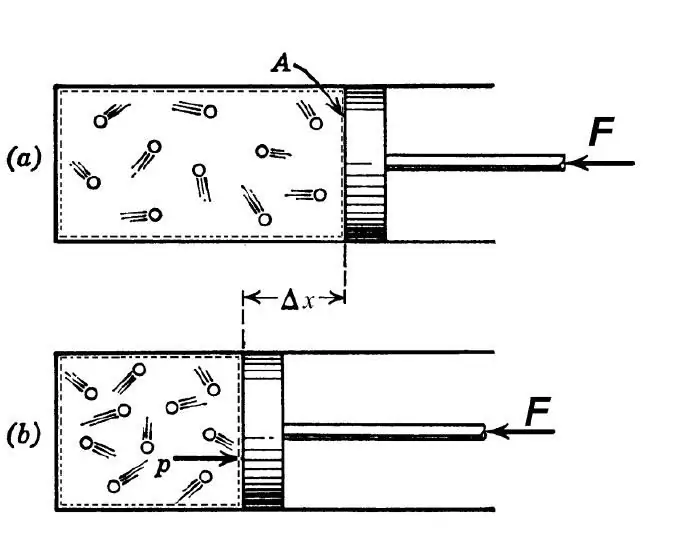
Adiabatický proces je podle termodynamické definice chápán jako takový přechod mezi počátečním a konečným stavem systému, v jehož důsledku nedochází k výměně tepla mezi vnějším prostředím a zkoumaným systémem. Takový proces je možný za následujících dvou podmínek:
- tepelná vodivost mezi vnějším prostředím asystém je z toho či onoho důvodu slabý;
- rychlost procesu je vysoká, takže výměna tepla nestihne nastat.
V strojírenství se adiabatický přechod používá jak k zahřátí plynu při jeho prudkém stlačení, tak k jeho ochlazení při rychlé expanzi. V přírodě se dotyčný termodynamický přechod projevuje, když vzduchová hmota stoupá nebo klesá ze svahu. Takové vzestupy a pády vedou ke změně rosného bodu ve vzduchu a srážek.
Poissonova rovnice pro adiabatický ideální plyn

Ideální plyn je systém, ve kterém se částice pohybují náhodně vysokou rychlostí, neinteragují spolu a jsou bezrozměrné. Takový model je velmi jednoduchý, pokud jde o jeho matematický popis.
Podle definice adiabatického procesu lze v souladu s prvním zákonem termodynamiky napsat následující výraz:
dU=-PdV.
Jinými slovy, plyn, expandující nebo smršťující, pracuje PdV díky odpovídající změně jeho vnitřní energie dU.
V případě ideálního plynu, pokud použijeme stavovou rovnici (Clapeyron-Mendelejevův zákon), můžeme dostat následující výraz:
PVγ=const.
Tato rovnost se nazývá Poissonova rovnice. Lidé, kteří jsou obeznámeni s fyzikou plynů, si všimnou, že pokud je hodnota γ rovna 1, pak Poissonova rovnice přejde do Boyle-Mariotteova zákona (izotermníproces). Taková transformace rovnic je však nemožná, protože γ pro jakýkoli typ ideálního plynu je větší než jedna. Veličina γ (gama) se nazývá adiabatický index ideálního plynu. Podívejme se blíže na jeho fyzický význam.
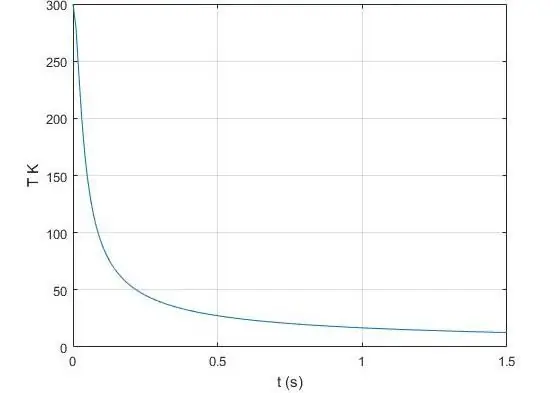
Co je adiabatický exponent?
Exponent γ, který se objevuje v Poissonově rovnici pro ideální plyn, je poměr tepelné kapacity při konstantním tlaku ke stejné hodnotě, ale již při konstantním objemu. Ve fyzice je tepelná kapacita množství tepla, které musí být přeneseno nebo odebráno danému systému, aby změnil svou teplotu o 1 Kelvin. Izobarickou tepelnou kapacitu budeme označovat symbolem CP a izochorickou tepelnou kapacitu symbolem CV. Pak platí rovnost pro γ:
γ=CP/CV.
Protože γ je vždy větší než jedna, ukazuje, kolikrát izobarická tepelná kapacita studovaného plynového systému překračuje podobnou izochorickou charakteristiku.
Tepelné kapacity CP a CV
K určení adiabatického exponentu by člověk měl dobře rozumět významu veličin CP a CV. K tomu provedeme následující myšlenkový experiment: představte si, že plyn je v uzavřeném systému v nádobě s pevnými stěnami. Pokud je nádoba zahřátá, pak se veškeré sdělované teplo v ideálním případě přemění na vnitřní energii plynu. V takové situaci bude platit rovnost:
dU=CVdT.
HodnotaCVdefinuje množství tepla, které musí být přeneseno do systému, aby bylo izochoricky ohřáto o 1 K.
Nyní předpokládejme, že plyn je v nádobě s pohyblivým pístem. V procesu zahřívání takového systému se píst bude pohybovat, což zajišťuje udržování konstantního tlaku. Protože entalpie systému v tomto případě bude rovna součinu izobarické tepelné kapacity a změny teploty, první termodynamický zákon bude mít tvar:
CPdT=CVdT + PdV.
Zde je vidět, že CP>CV, protože v případě izobarické změny stavů je nutné utrácet teplo nejen za účelem zvýšení teploty systému, a tím i jeho vnitřní energie, ale také práce, kterou plyn vykoná při jeho expanzi.
Hodnota γ pro ideální monoatomický plyn
Nejjednodušší plynový systém je monatomický ideální plyn. Předpokládejme, že máme 1 mol takového plynu. Připomeňme, že v procesu izobarického ohřevu 1 molu plynu o pouhý 1 Kelvin funguje stejně jako R. Tento symbol se běžně používá k označení univerzální plynové konstanty. Je to rovno 8,314 J / (molK). Aplikováním posledního výrazu v předchozím odstavci pro tento případ dostaneme následující rovnost:
CP=CV+ R.
Odkud můžete určit hodnotu izochorické tepelné kapacity CV:
γ=CP/CV;
CV=R/(γ-1).
Je známo, že na jednoho krtkajednoatomový plyn, hodnota izochorické tepelné kapacity je:
CV=3/2R.
Z posledních dvou rovností vyplývá hodnota adiabatického exponentu:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Všimněte si, že hodnota γ závisí výhradně na vnitřních vlastnostech plynu samotného (na polyatomické povaze jeho molekul) a nezávisí na množství látky v systému.
Závislost γ na počtu stupňů volnosti
Rovnice pro izochorickou tepelnou kapacitu jednoatomového plynu byla napsána výše. Koeficient 3/2, který se v něm objevil, souvisí s počtem stupňů volnosti v jednom atomu. Má schopnost pohybovat se pouze v jednom ze tří směrů prostoru, to znamená, že existují pouze translační stupně volnosti.
Pokud je systém tvořen dvouatomovými molekulami, pak se ke třem translačním přidají další dva rotační stupně. Proto výraz pro CV bude:
CV=5/2R.
Pak hodnota γ bude:
γ=7/5=1, 4.
Všimněte si, že dvouatomová molekula má ve skutečnosti ještě jeden vibrační stupeň volnosti, ale při teplotách několika stovek Kelvinů se neaktivuje a nepřispívá k tepelné kapacitě.
Pokud se molekuly plynu skládají z více než dvou atomů, budou mít 6 stupňů volnosti. Adiabatický exponent bude v tomto případě roven:
γ=4/3 ≈ 1, 33.
TakžeS rostoucím počtem atomů v molekule plynu tedy klesá hodnota γ. Pokud vytvoříte adiabatický graf v osách P-V, všimnete si, že křivka pro monoatomický plyn se bude chovat ostřeji než pro polyatomický.
Adiabatický exponent pro směs plynů
Výše jsme ukázali, že hodnota γ nezávisí na chemickém složení plynového systému. Záleží však na počtu atomů, které tvoří jeho molekuly. Předpokládejme, že systém se skládá z N komponent. Atomový podíl složky i ve směsi je ai. K určení adiabatického exponentu směsi pak můžete použít následující výraz:
γ=∑i=1N(aiγ i).
Kde γi je hodnota γ pro i-tou složku.
Tento výraz lze například použít k určení γ vzduchu. Vzhledem k tomu, že se skládá z 99 % dvouatomových molekul kyslíku a dusíku, měl by se jeho adiabatický index velmi blížit hodnotě 1,4, což potvrzuje i experimentální stanovení této hodnoty.






