Adiabatický přechod mezi dvěma skupenstvími v plynech nepatří mezi izoprocesy, hraje však důležitou roli nejen v různých technologických procesech, ale i v přírodě. V tomto článku se zamyslíme nad tím, co tento proces je, a také uvedeme adiabatické rovnice pro ideální plyn.
Ideální plyn ve zkratce
Ideální plyn je takový, ve kterém neexistují žádné interakce mezi jeho částicemi a jejich velikost je rovna nule. V přírodě samozřejmě žádné stoprocentně ideální plyny neexistují, protože všechny jsou složeny z molekul a atomů o velikosti, které spolu vždy interagují alespoň pomocí van der Waalsových sil. Nicméně popsaný model je často prováděn s dostatečnou přesností pro řešení praktických problémů pro mnoho reálných plynů.
Hlavní rovnicí ideálního plynu je Clapeyron-Mendělejevův zákon. Píše se v následujícím tvaru:
PV=nRT.
Tato rovnice stanoví přímou úměrnost mezi produktemtlak P na objemu V a množství látky n na absolutní teplotě T. Hodnota R je plynová konstanta, která hraje roli faktoru úměrnosti.
Co je adiabatický proces?
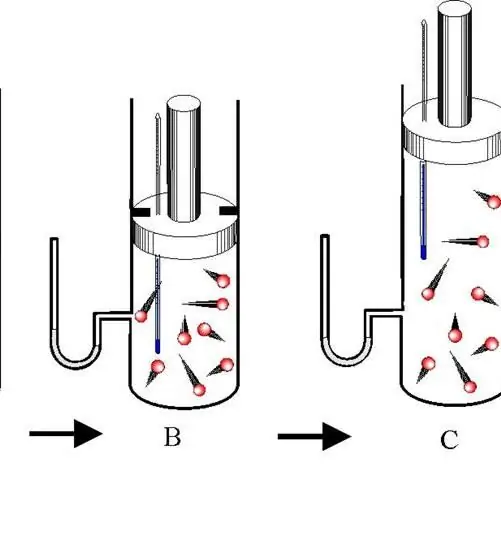
Adiabatický proces je přechod mezi stavy plynového systému, ve kterém nedochází k výměně energie s prostředím. V tomto případě se všechny tři termodynamické charakteristiky systému (P, V, T) mění a množství látky n zůstává konstantní.
Rozlišujte mezi adiabatickou expanzí a kontrakcí. Oba procesy probíhají pouze díky vnitřní energii systému. Takže v důsledku expanze dramaticky klesá tlak a zejména teplota systému. Naopak adiabatická komprese má za následek pozitivní skok v teplotě a tlaku.
Aby se zabránilo výměně tepla mezi okolím a systémem, musí mít tento systém tepelně izolované stěny. Kromě toho zkrácení doby procesu výrazně snižuje tok tepla do a ze systému.
Poissonovy rovnice pro adiabatický proces

První termodynamický zákon je napsán takto:
Q=ΔU + A.
Jinými slovy, teplo Q sdělené systému se používá k vykonání práce A systémem a ke zvýšení jeho vnitřní energie ΔU. Chcete-li napsat adiabatickou rovnici, měli byste dát Q=0, což odpovídá definici studovaného procesu. Dostáváme:
ΔU=-A.
S izochorickýmprocesu v ideálním plynu jde všechno teplo ke zvýšení vnitřní energie. Tato skutečnost nám umožňuje zapsat rovnost:
ΔU=CVΔT.
Kde CV je izochorická tepelná kapacita. Práce A se zase vypočítá takto:
A=PdV.
Kde dV je malá změna hlasitosti.
Kromě Clapeyron-Mendelejevovy rovnice platí pro ideální plyn následující rovnice:
CP- CV=R.
Kde CP je izobarická tepelná kapacita, která je vždy větší než izochorická, protože bere v úvahu ztráty plynu v důsledku expanze.
Analýzou výše napsaných rovnic a integrací přes teplotu a objem dojdeme k následující adiabatické rovnici:
TVγ-1=const.
Zde je γ adiabatický index. Rovná se poměru izobarické tepelné kapacity k izochorické. Tato rovnost se nazývá Poissonova rovnice pro adiabatický proces. Použitím Clapeyron-Mendelejevova zákona můžete napsat další dva podobné výrazy, pouze pomocí parametrů P-T a P-V:
TPγ/(γ-1)=const;
PVγ=const.
Adiabatický graf může být uveden v různých osách. Níže je zobrazeno v osách P-V.
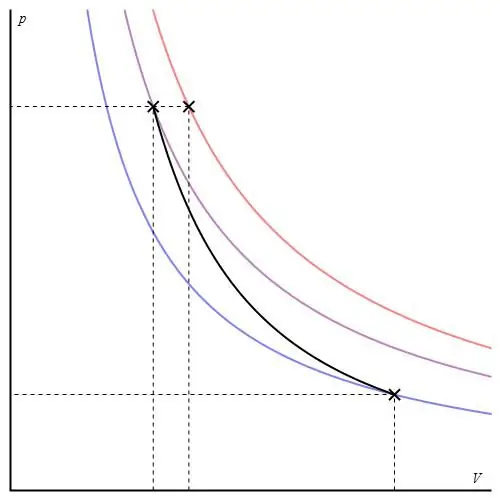
Barevné čáry v grafu odpovídají izotermám, černá křivka je adiabat. Jak je vidět, adiabat se chová ostřeji než kterákoli z izoterm. Tuto skutečnost lze snadno vysvětlit: pro izotermu se tlak mění zpětúměrné objemu, ale pro izobatu se tlak mění rychleji, protože exponent je γ>1 pro jakýkoli plynový systém.
Příklad problému
V přírodě, v horských oblastech, když se vzduchová hmota pohybuje po svahu, klesá její tlak, zvětšuje svůj objem a ochlazuje se. Tento adiabatický proces snižuje rosný bod a vytváří kapalné a pevné srážky.

Navrhuje se vyřešit následující problém: v procesu zvedání vzduchové hmoty podél svahu hory poklesl tlak o 30 % ve srovnání s tlakem na úpatí. Jaká byla jeho teplota, pokud na úpatí byla 25 oC?
Pro vyřešení problému použijte následující adiabatickou rovnici:
TPγ/(γ-1)=const.
Je lepší to napsat v tomto tvaru:
T2/T1=(P2/P 1)(γ-1)/γ.
Pokud se P1 bere jako 1 atmosféra, pak P2 bude rovno 0,7 atmosféry. Pro vzduch je adiabatický index 1,4, protože jej lze považovat za dvouatomový ideální plyn. Hodnota teploty T1 je 298,15 K. Dosazením všech těchto čísel do výše uvedeného výrazu dostaneme T2=269,26 K, což odpovídá - 3, 9 oC.






