Tepelná kapacita plynu je množství energie, kterou tělo absorbuje, když je zahřáté o jeden stupeň. Pojďme analyzovat hlavní charakteristiky této fyzikální veličiny.

Definice
Měrné teplo plynu je jednotková hmotnost konkrétní látky. Jeho jednotky měření jsou J/(kg·K). Množství tepla, které je absorbováno tělem v procesu změny jeho stavu agregace, je spojeno nejen s počátečním a konečným stavem, ale také se způsobem přechodu.

Oddělení
Tepelná kapacita plynů se dělí hodnotou určenou při konstantním objemu (Cv), konstantním tlaku (Cр).
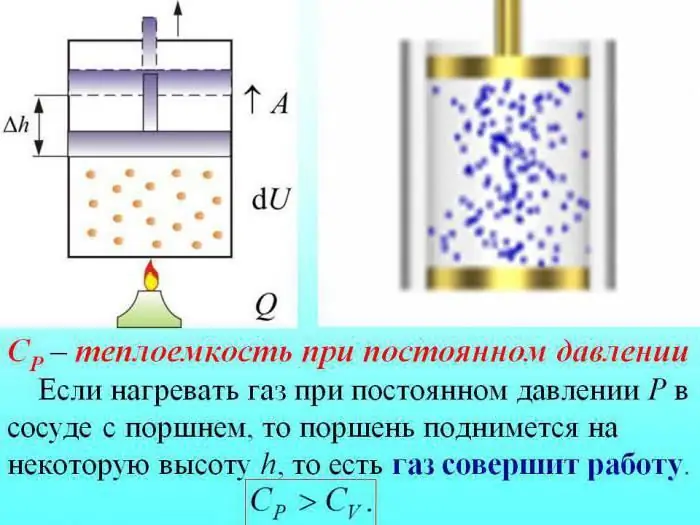
V případě ohřevu beze změny tlaku se určité množství tepla spotřebuje na práci expanze plynu a část energie se spotřebuje na zvýšení vnitřní energie.
Tepelná kapacita plynů při konstantním tlaku je určena množstvím tepla, které se spotřebuje na zvýšení vnitřní energie.
Stav plynu: vlastnosti, popis
Tepelná kapacita ideálního plynu je určena s ohledem na skutečnost, že Сp-Сv=R. Poslední veličina se nazývá univerzální plynová konstanta. Jeho hodnota odpovídá 8,314 J/(mol K).
Při provádění teoretických výpočtů tepelné kapacity, například při popisu vztahu s teplotou, nestačí používat pouze termodynamické metody, je důležité vyzbrojit se prvky statické fyziky.
Tepelná kapacita plynů zahrnuje výpočet průměrné hodnoty energie translačního pohybu některých molekul. Takový pohyb je sčítán z rotačního a translačního pohybu molekuly, jakož i z vnitřních vibrací atomů.
Ve statické fyzice existuje informace, že pro každý stupeň volnosti rotačního a translačního pohybu existuje množství plynu, které se rovná polovině univerzální plynové konstanty.

Zajímavá fakta
Předpokládá se, že částice monatomického plynu má tři translační stupně volnosti, takže měrné teplo plynu má tři translační, dva rotační a jeden vibrační stupeň volnosti. Zákon jejich rovnoměrného rozdělení vede k přirovnání měrného tepla při konstantním objemu k R.
Během experimentů bylo zjištěno, že tepelná kapacita dvouatomového plynu odpovídá hodnotě R. Takový rozpor mezi teorií a praxí se vysvětluje tím, že tepelná kapacita ideálního plynu je spojena s kvantem efektů, proto je při výpočtech důležité používat statistiky založené na kvantmechanika.
Na základech kvantové mechaniky má jakýkoli systém částic, které oscilují nebo rotují, včetně molekul plynu, pouze určité diskrétní hodnoty energie.
Pokud energie tepelného pohybu v systému nestačí k vybuzení oscilací určité frekvence, takové pohyby nepřispívají k celkové tepelné kapacitě systému.
V důsledku toho se určitý stupeň volnosti „zamrzne“, není možné na něj aplikovat zákon ekvipartice.
Tepelná kapacita plynů je důležitou charakteristikou stavu, na kterém závisí fungování celého termodynamického systému.
Teplota, při které lze zákon equipartition aplikovat na vibrační nebo rotační stupeň volnosti, je charakterizována kvantovou teorií, spojuje Planckovu konstantu s Boltzmannovou konstantou.

Diatomické plyny
Mezery mezi úrovněmi rotační energie takových plynů jsou malé množství stupňů. Výjimkou je vodík, ve kterém je hodnota teploty určena stovkami stupňů.
To je důvod, proč je obtížné popsat tepelnou kapacitu plynu při konstantním tlaku zákonem rovnoměrného rozdělení. V kvantové statistice se při určování tepelné kapacity bere v úvahu, že její vibrační část v případě poklesu teploty rychle klesá a dosahuje nuly.
Tento jev vysvětluje skutečnost, že při pokojové teplotě prakticky neexistuje žádná vibrační část tepelné kapacity, např.dvouatomový plyn, odpovídá konstantě R.
Tepelná kapacita plynu při konstantním objemu v případě indikátorů nízké teploty se určuje pomocí kvantové statistiky. Existuje Nernstův princip, který se nazývá třetí termodynamický zákon. Na základě jeho formulace se molární tepelná kapacita plynu bude s klesající teplotou snižovat až k nule.

Vlastnosti pevných látek
Pokud lze tepelnou kapacitu směsi plynů vysvětlit pomocí kvantové statistiky, pak pro pevný stav agregace je tepelný pohyb charakterizován mírnými fluktuacemi částic v blízkosti rovnovážné polohy.
Každý atom má tři vibrační stupně volnosti, proto v souladu se zákonem o ekvipartici lze molární tepelnou kapacitu pevné látky vypočítat jako 3nR, kde n je počet atomů v molekule.
V praxi je toto číslo limitem, ke kterému má tepelná kapacita pevného tělesa tendenci při vysokých teplotách.
U některých prvků, včetně kovů, lze maximum získat při běžných teplotách. Pro n=1 je Dulongův a Petitův zákon splněn, ale pro složité látky je dosti obtížné takového limitu dosáhnout. Protože limit nelze ve skutečnosti získat, dochází k rozkladu nebo tání pevné látky.
Historie kvantové teorie
Zakladateli kvantové teorie jsou Einstein a Debye na začátku dvacátého století. Je založena na kvantování oscilačních pohybů atomů v určitémkrystal. U nízkoteplotních indikátorů se ukazuje, že tepelná kapacita pevného tělesa je přímo úměrná absolutní kubické hodnotě. Tento vztah se nazývá Debyeův zákon. Jako kritérium, které umožňuje rozlišit mezi indikátory nízké a vysoké teploty, se bere jejich srovnání s teplotou Debye.
Tato hodnota je určena spektrem vibrací atomu v těle, proto velmi závisí na vlastnostech jeho krystalové struktury.
QD je hodnota, která má několik set K, ale například u diamantu je mnohem vyšší.
Vodivé elektrony významně přispívají k tepelné kapacitě kovů. K jeho výpočtu se používá Fermiho kvantová statistika. Elektronová vodivost pro atomy kovů je přímo úměrná absolutní teplotě. Protože se jedná o nevýznamnou hodnotu, bere se v úvahu pouze při teplotách směřujících k absolutní nule.
Metody pro stanovení tepelné kapacity
Hlavní experimentální metodou je kalorimetrie. K provedení teoretického výpočtu tepelné kapacity se používá statistická termodynamika. Platí pro ideální plyn i pro krystalická tělesa, provádí se na základě experimentálních dat o struktuře hmoty.
Empirické metody pro výpočet tepelné kapacity ideálního plynu jsou založeny na myšlence chemické struktury, příspěvku jednotlivých skupin atomů k Ср.
U kapalin se také používají metody, které jsou založeny na použití termodynamikycykly, které umožňují přejít z tepelné kapacity ideálního plynu do kapaliny prostřednictvím derivace teploty entalpie procesu odpařování.
V případě řešení není výpočet tepelné kapacity jako aditivní funkce povolen, protože nadbytečná hodnota tepelné kapacity řešení je v zásadě významná.
K jejímu vyhodnocení potřebujeme molekulárně-statistickou teorii řešení. Nejobtížnější je identifikace tepelné kapacity heterogenních systémů v termodynamické analýze.

Závěr
Studium tepelné kapacity umožňuje vypočítat energetickou bilanci procesů probíhajících v chemických reaktorech i v jiných chemických výrobních zařízeních. Tato hodnota je navíc nezbytná pro výběr optimálních typů chladicích kapalin.
V současné době je experimentální stanovení tepelné kapacity látek pro různé teplotní intervaly - od nízkých hodnot po vysoké hodnoty - hlavní možností pro stanovení termodynamických charakteristik látky. Při výpočtu entropie a entalpie látky se používají integrály tepelné kapacity. Informace o tepelné kapacitě chemických činidel v určitém teplotním rozsahu umožňuje vypočítat tepelný účinek procesu. Informace o tepelné kapacitě roztoků umožňuje vypočítat jejich termodynamické parametry při libovolných hodnotách teplot v rámci analyzovaného intervalu.
Například kapalina je charakterizována výdejem části tepla na změnu hodnoty potenciální energiereagující molekuly. Tato hodnota se nazývá „konfigurační“tepelná kapacita, která se používá k popisu řešení.
Je obtížné provádět plnohodnotné matematické výpočty bez zohlednění termodynamických charakteristik látky, jejího stavu agregace. Proto se pro kapaliny, plyny, pevné látky používá taková charakteristika, jako je měrná tepelná kapacita, která umožňuje charakterizovat energetické parametry látky.






